Trente-neuf mille milliards de bactéries vivent dans votre intestin, formant un écosystème d'une complexité comparable à une forêt tropicale. Cet « organe invisible » — le microbiote intestinal — est au cœur d'une révolution médicale. Digestion, immunité, métabolisme, santé mentale : les découvertes s'accumulent et transforment notre compréhension du corps humain. Plongée dans un monde microscopique aux effets macroscopiques.
Sommaire
La découverte d'un organe invisible
L'histoire de la découverte du microbiote intestinal est celle d'un changement de paradigme en biologie. Pendant des siècles, les bactéries ont été perçues uniquement comme des agents pathogènes à combattre. Pasteur et Koch, pères de la microbiologie, ont sauvé des millions de vies en identifiant les bactéries responsables de maladies infectieuses, mais cette vision « guerre contre les microbes » a eu un effet collatéral : elle a masqué le rôle fondamental des bactéries bénéfiques qui vivent en symbiose avec nous.
Le tournant est venu avec le Human Microbiome Project, lancé en 2007 par les National Institutes of Health américains. Ce projet pharaonique visait à caractériser l'ensemble des communautés microbiennes associées au corps humain. Les résultats, publiés en 2012, ont été stupéfiants : le corps humain héberge au moins autant de cellules bactériennes que de cellules humaines, et le génome collectif de ces bactéries — le métagénome — contient 150 fois plus de gènes que le génome humain. Nous ne sommes pas des organismes isolés mais des « superorganismes », des écosystèmes ambulants.
La révolution technologique du séquençage génomique à haut débit a été le catalyseur de cette découverte. Avant les années 2000, l'étude du microbiote se limitait aux bactéries cultivables en laboratoire, soit environ 20 % du total. Les techniques de séquençage de l'ARN ribosomal 16S, puis la métagénomique shotgun, ont permis d'identifier la totalité des micro-organismes présents, y compris les 80 % non cultivables. En quelques années, notre connaissance du microbiote est passée de l'esquisse à une carte de plus en plus détaillée.
Le saviez-vous ? Le microbiote intestinal pèse environ 1,5 kg — autant que le cerveau. Et comme le cerveau, il est unique à chaque individu : la composition du microbiote varie davantage entre deux personnes qu'entre les génomes de deux êtres humains quelconques. On parle d'empreinte microbienne, aussi distinctive qu'une empreinte digitale.
Composition et diversité du microbiote
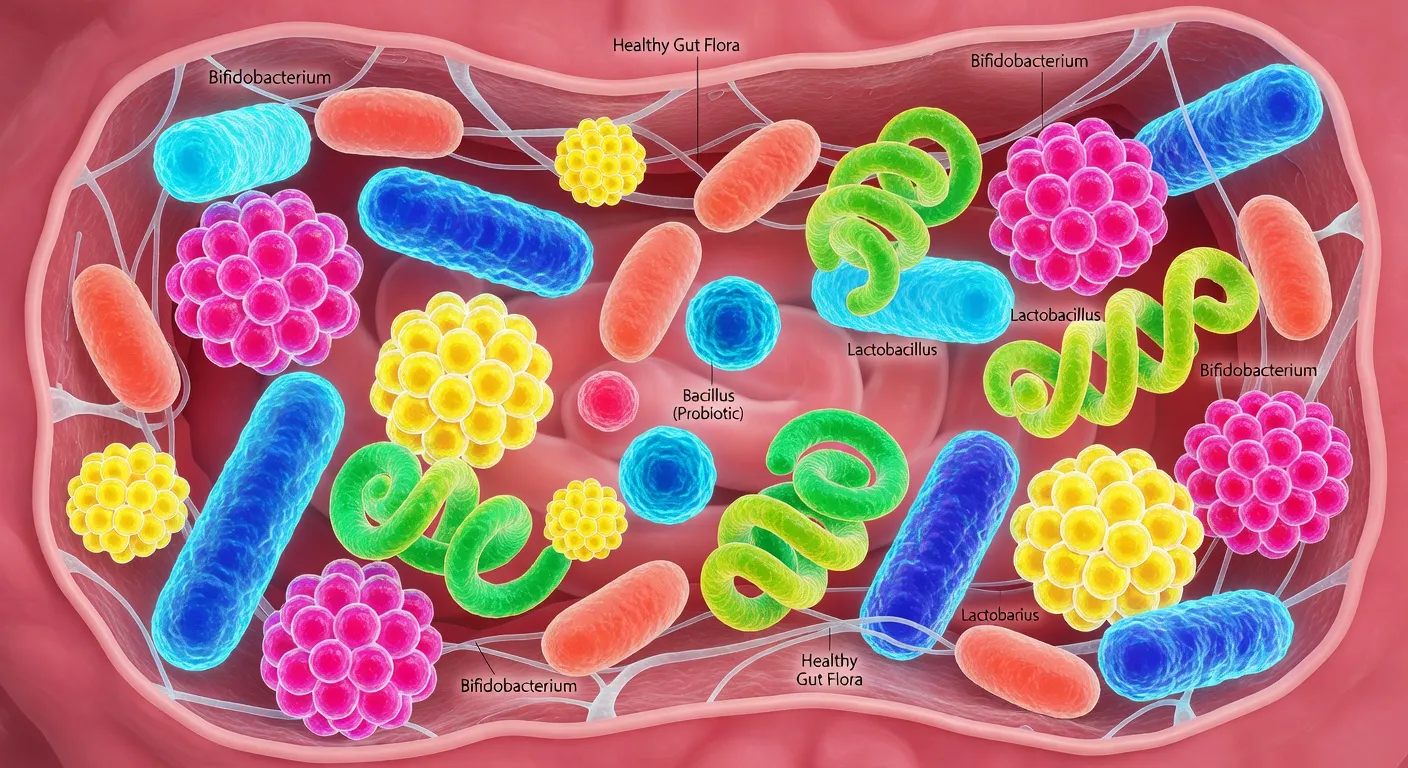
Le microbiote intestinal est un écosystème d'une diversité remarquable. Il comprend principalement des bactéries, mais aussi des archées (des micro-organismes proches des bactéries), des virus (principalement des bactériophages qui infectent les bactéries), des champignons (le mycobiote) et des protistes. Parmi les bactéries, deux phyla dominent : les Firmicutes et les Bacteroidetes, qui représentent ensemble plus de 90 % des bactéries intestinales. Le ratio entre ces deux groupes est un indicateur de santé métabolique étudié de près par les chercheurs.
La diversité du microbiote — le nombre d'espèces différentes présentes — est considérée comme un marqueur de santé. Un microbiote diversifié est plus résilient face aux perturbations (antibiotiques, changements alimentaires, infections) et remplit mieux ses fonctions métaboliques. Les populations occidentales présentent un microbiote significativement moins diversifié que les populations rurales d'Afrique ou d'Amérique du Sud, une différence attribuée à l'alimentation ultra-transformée, à l'usage d'antibiotiques et au mode de vie urbain.
La composition du microbiote se met en place dès la naissance et subit des évolutions majeures au cours de la vie. Le mode d'accouchement joue un rôle fondamental : les bébés nés par voie basse sont colonisés par les bactéries vaginales et fécales de la mère (Lactobacillus, Bacteroides), tandis que ceux nés par césarienne sont d'abord colonisés par des bactéries de la peau et de l'environnement hospitalier (Staphylococcus, Clostridium). Ces différences initiales persistent pendant les premiers mois et peuvent avoir des conséquences immunologiques à long terme.
L'allaitement maternel est le second facteur déterminant. Le lait maternel contient non seulement des bactéries bénéfiques (Bifidobacterium, Lactobacillus) mais aussi des oligosaccharides — des sucres complexes non digestibles par le nourrisson mais qui servent de nourriture sélective à ces bactéries bénéfiques. La nature a conçu un système d'une élégance remarquable pour ensemencer et nourrir le microbiote du nouveau-né.
L'appauvrissement moderne du microbiote
L'une des hypothèses les plus débattues en médecine contemporaine est l'hypothèse de la « disparition du microbiote » formulée par Martin Blaser. Selon cette théorie, l'usage massif d'antibiotiques depuis les années 1940, combiné aux changements alimentaires (moins de fibres, plus de produits ultra-transformés) et au mode de vie aseptisé des sociétés industrialisées, aurait provoqué une perte progressive de diversité microbienne d'une génération à l'autre. Cette perte cumulative pourrait contribuer à l'explosion des maladies chroniques modernes : allergies, maladies auto-immunes, obésité, diabète.
Les données ethnographiques soutiennent cette hypothèse. Le peuple Yanomami du Venezuela, contacté pour la première fois en 2009 et n'ayant jamais été exposé aux antibiotiques ni à l'alimentation occidentale, possède le microbiote le plus diversifié jamais mesuré chez l'humain — environ deux fois plus diversifié que celui d'un Américain moyen. Cette diversité perdue ne peut être retrouvée simplement en changeant d'alimentation : certaines espèces bactériennes semblent avoir été irrémédiablement perdues dans les populations occidentales.
Les fonctions digestives et métaboliques
La fonction la plus intuitive du microbiote intestinal est la digestion. Nos enzymes digestives sont incapables de décomposer certains glucides complexes — les fibres alimentaires — qui parviennent intacts jusqu'au côlon. C'est là que les bactéries intestinales prennent le relais, fermentant ces fibres pour produire des acides gras à chaîne courte (AGCC) : butyrate, propionate et acétate. Ces métabolites, loin d'être de simples déchets, sont des molécules biologiquement actives aux fonctions multiples.
Le butyrate est la principale source d'énergie des cellules de la muqueuse colique (les colonocytes). Il maintient l'intégrité de la barrière intestinale, réduit l'inflammation locale et possède des propriétés anti-tumorales documentées. Une production insuffisante de butyrate, liée à un régime pauvre en fibres, fragilise la barrière intestinale et contribue au phénomène de « leaky gut » (hyperperméabilité intestinale), qui laisse passer des molécules bactériennes dans la circulation sanguine et provoque une inflammation systémique chronique de bas grade.
Le propionate est transporté au foie où il influence le métabolisme du glucose et du cholestérol. L'acétate est utilisé comme source d'énergie par les tissus périphériques et influence la régulation de l'appétit via des récepteurs hypothalamiques. Ensemble, ces trois AGCC constituent un réseau de signalisation métabolique dont on commence seulement à mesurer l'importance.
Le microbiote synthétise également des vitamines essentielles que notre organisme ne peut pas produire seul : vitamine K (indispensable à la coagulation sanguine), vitamines B12, B9 (folate), B2 et B7 (biotine). Cette production microbienne couvre une partie significative de nos besoins quotidiens et explique pourquoi un traitement antibiotique prolongé peut entraîner des carences vitaminiques.
En Drôme. La Drôme, avec sa tradition agricole biologique (premier département bio de France en surface cultivée), offre un accès privilégié aux aliments riches en fibres diversifiées. Les marchés de producteurs de Nyons, Die, Crest ou Valence permettent de trouver des fruits et légumes de variétés anciennes, dont la richesse en fibres et en polyphénols est supérieure à celle des variétés industrielles standardisées — un atout direct pour la diversité du microbiote.
Microbiote et système immunitaire
Le lien entre le microbiote intestinal et le système immunitaire est si profond que de nombreux immunologistes considèrent aujourd'hui le microbiote comme un organe immunitaire à part entière. Et les chiffres donnent le vertige : l'intestin abrite environ 70 % des cellules immunitaires du corps humain, concentrées dans le tissu lymphoïde associé à l'intestin (GALT pour Gut-Associated Lymphoid Tissue). Pour comprendre le lien entre environnement et santé dans notre région, consultez notre guide santé-environnement en Drôme.
Le microbiote joue un rôle crucial dans l'éducation du système immunitaire. Dès la naissance, les bactéries intestinales « forment » les cellules immunitaires à distinguer le soi du non-soi, le dangereux de l'inoffensif. Les souris axéniques (élevées en environnement stérile, sans microbiote) présentent un système immunitaire gravement déficient : ganglions lymphatiques atrophiés, production d'anticorps effondrée, susceptibilité accrue aux infections. La restauration d'un microbiote normal corrige ces anomalies, démontrant le rôle causal des bactéries dans le développement immunitaire.
L'hypothèse hygiéniste, formulée en 1989 par David Strachan, propose que l'augmentation des allergies et des maladies auto-immunes dans les pays industrialisés s'explique par une diminution de l'exposition aux micro-organismes dans l'enfance. L'excès d'hygiène, la réduction de la taille des familles, le recul de l'allaitement et l'usage d'antibiotiques priveraient le système immunitaire des stimulations nécessaires à sa maturation. Un système immunitaire insuffisamment « éduqué » aurait tendance à réagir de manière disproportionnée à des substances inoffensives (allergènes) ou à ses propres tissus (auto-immunité).
Dysbiose et maladies inflammatoires
La dysbiose — un déséquilibre de la composition du microbiote — est associée à un nombre croissant de pathologies. Les maladies inflammatoires chroniques de l'intestin (MICI) — maladie de Crohn et rectocolite hémorragique — sont celles où le lien est le plus solidement établi. Les patients atteints de MICI présentent systématiquement un microbiote appauvri, avec une diminution des bactéries productrices de butyrate et une augmentation des espèces pro-inflammatoires.
Le syndrome de l'intestin irritable (SII), qui touche 10 à 15 % de la population, est également associé à des anomalies du microbiote, bien que le tableau soit plus complexe que dans les MICI. Les études sur la transplantation de microbiote fécal (TMF) — le transfert du microbiote d'un donneur sain vers un patient — ont montré des résultats prometteurs dans certains cas de SII, confirmant le rôle causal du microbiote dans cette pathologie.
La TMF est d'ores et déjà un traitement validé pour les infections récidivantes à Clostridioides difficile, une bactérie qui profite de la dévastation du microbiote par les antibiotiques pour proliférer et provoquer des colites potentiellement mortelles. Le taux de guérison de la TMF dépasse 90 % pour cette indication, contre 30 % pour les antibiotiques seuls. Ce succès spectaculaire a ouvert la voie à des essais cliniques pour de nombreuses autres pathologies, de l'obésité à la maladie de Parkinson.
L'axe intestin-cerveau : quand les bactéries parlent au cerveau
La découverte la plus surprenante de la recherche sur le microbiote concerne probablement ses effets sur le cerveau et le comportement. L'axe intestin-cerveau est un système de communication bidirectionnel qui utilise plusieurs voies : le nerf vague (le plus long nerf crânien, qui connecte directement l'intestin au tronc cérébral), le système immunitaire, les hormones intestinales et les métabolites bactériens qui traversent la barrière hémato-encéphalique.
L'expérience fondatrice a été réalisée en 2004 par l'équipe de Nobuyuki Sudo au Japon : des souris axéniques (sans microbiote) présentaient une réponse au stress exagérée par rapport aux souris normales, un effet qui pouvait être corrigé par la colonisation avec une seule espèce bactérienne (Bifidobacterium infantis), mais uniquement si cette colonisation avait lieu pendant une fenêtre critique précoce. Cette étude a démontré pour la première fois que les bactéries intestinales influencent directement le fonctionnement cérébral.
Depuis, les découvertes se sont multipliées. Le microbiote intestinal produit environ 95 % de la sérotonine du corps (via les cellules entérochromaffines de l'intestin), un neurotransmetteur clé dans la régulation de l'humeur, du sommeil et de l'appétit. Il produit également du GABA (neurotransmetteur inhibiteur), de la dopamine (motivation, récompense) et de l'acétylcholine (cognition). Les liens entre microbiote et fonctions cérébrales sont aujourd'hui un champ de recherche parmi les plus actifs en neurosciences.

En psychiatrie, les données s'accumulent. Les patients souffrant de dépression majeure présentent un microbiote significativement différent de celui des personnes saines, avec une diminution de certaines espèces productrices de butyrate et de GABA. Des essais cliniques de « psychobiotiques » — des probiotiques ciblant spécifiquement la santé mentale — montrent des résultats encourageants sur les symptômes anxieux et dépressifs légers à modérés, bien que la recherche en soit encore à ses débuts.
Le saviez-vous ? L'intestin possède son propre système nerveux, le système nerveux entérique, qui contient environ 500 millions de neurones — davantage que la moelle épinière. Ce « deuxième cerveau » est capable de fonctionner de manière autonome, contrôlant la motricité intestinale, la sécrétion d'enzymes et le flux sanguin sans intervention du cerveau. Il communique en permanence avec le cerveau via le nerf vague, et les bactéries intestinales influencent directement son activité.
Préserver et enrichir son microbiote
Les connaissances accumulées sur le microbiote débouchent sur des recommandations pratiques pour entretenir cet écosystème intérieur. La bonne nouvelle est que le microbiote, bien qu'il soit influencé par des facteurs que nous ne contrôlons pas (génétique, mode de naissance, expositions précoces), est remarquablement sensible aux changements alimentaires et comportementaux. Des modifications significatives de la composition du microbiote peuvent être observées en aussi peu que 24 heures après un changement de régime.
La diversité alimentaire est le facteur le plus important. L'étude American Gut Project, qui a analysé le microbiote de plus de 10 000 personnes, a montré que les individus consommant plus de 30 plantes différentes par semaine (fruits, légumes, légumineuses, céréales, noix, graines, herbes aromatiques) avaient un microbiote significativement plus diversifié que ceux en consommant moins de 10. Chaque type de fibre nourrit des espèces bactériennes différentes, d'où l'importance de la variété.
Les aliments fermentés — yaourt, kéfir, choucroute, kimchi, miso, kombucha, fromages à pâte persillée — apportent des bactéries vivantes qui, même si elles ne s'implantent pas durablement dans l'intestin, stimulent le système immunitaire local et produisent des métabolites bénéfiques pendant leur transit. Une étude de Stanford publiée en 2021 a montré qu'un régime riche en aliments fermentés pendant 10 semaines augmentait la diversité du microbiote et réduisait les marqueurs d'inflammation systémique.
Les prébiotiques — des fibres non digestibles qui nourrissent sélectivement les bactéries bénéfiques — sont présents dans de nombreux aliments : ail, oignon, poireau, asperge, artichaut, banane verte, chicorée. L'inuline et les fructo-oligosaccharides (FOS) sont les mieux étudiés et favorisent la croissance des bifidobactéries et des lactobacilles, deux genres associés à une bonne santé intestinale.
Les probiotiques en compléments alimentaires peuvent être utiles dans certaines situations spécifiques : après un traitement antibiotique (pour accélérer la reconstitution du microbiote), en cas de syndrome de l'intestin irritable (certaines souches de Bifidobacterium et Lactobacillus ont montré une efficacité modeste) ou lors de voyages dans des zones à risque de turista. Le choix de la souche est crucial : tous les probiotiques ne sont pas équivalents, et l'efficacité démontrée pour une souche ne peut pas être extrapolée à une autre.
À l'inverse, certains facteurs appauvrissent le microbiote et méritent d'être limités. Les antibiotiques, bien qu'indispensables pour traiter les infections bactériennes, sont des bombes à fragmentation pour le microbiote. Un seul traitement de 7 jours peut réduire la diversité microbienne de 30 % et certaines espèces mettent des mois à se rétablir, si elles se rétablissent. L'alimentation ultra-transformée, riche en additifs (émulsifiants, édulcorants artificiels) et pauvre en fibres, modifie défavorablement la composition du microbiote en quelques jours. Le stress chronique, via l'axe hypothalamo-hypophyso-surrénalien, altère la perméabilité intestinale et modifie la composition microbienne.
En Drôme. Le Pôle agroalimentaire de Valence et l'INRAE de Montpellier (qui couvre la région sud-est) mènent des recherches sur les liens entre alimentation, terroir et microbiote. Les produits drômois traditionnels — picodon (fromage de chèvre), clairette de Die (vin effervescent naturel), olives de Nyons — sont des aliments fermentés dont les communautés microbiennes spécifiques font l'objet d'études pour comprendre leur impact sur le microbiote des consommateurs.
La recherche sur le microbiote intestinal avance à une vitesse vertigineuse. Chaque mois, des centaines de nouvelles études sont publiées, affinant notre compréhension de cet écosystème intérieur et de ses interactions avec l'ensemble de notre physiologie. Si de nombreuses questions restent ouvertes — comment définir un microbiote « sain » ? Les transplantations de microbiote deviendront-elles un traitement de routine ? Pourra-t-on modifier durablement un microbiote appauvri ? — une certitude émerge : prendre soin de ses bactéries intestinales, c'est prendre soin de sa santé globale, du système digestif au cerveau en passant par le système immunitaire. Le microbiote est véritablement l'organe invisible qui gouverne notre bien-être.